Η αναβίωση των μπαταριών ιόντων νατρίου σε θερμοκρασία δωματίου
Λόγω των άφθονων αποθεμάτων νατρίου (Na) στον φλοιό της Γης και των παρόμοιων φυσικοχημικών ιδιοτήτων του νατρίου και του λιθίου, η αποθήκευση ηλεκτροχημικής ενέργειας με βάση το νάτριο υπόσχεται σημαντική αποθήκευση ενέργειας και ανάπτυξη δικτύου. Για παράδειγμα, κυψέλες ερευνητικής δραστηριότητας μπαταριών μηδενικών εκπομπών υψηλής θερμοκρασίας που βασίζονται σε συστήματα Na/NiCl2 και κυψέλες Na–S υψηλής θερμοκρασίας, που είναι επιτυχημένες εμπορικές περιπτώσεις σταθερών και φορητών εφαρμογών, έχουν ήδη αποδείξει τις δυνατότητες των επαναφορτιζόμενων μπαταριών με βάση το νάτριο. Ωστόσο, η υψηλή θερμοκρασία λειτουργίας τους περίπου 300 °C προκαλεί προβλήματα ασφάλειας και μειώνει την απόδοση μετ' επιστροφής των μπαταριών ιόντων νατρίου (SIB). Ως εκ τούτου, τα SIB θερμοκρασίας δωματίου (RT) θεωρούνται ευρέως ως η πιο υποσχόμενη εναλλακτική τεχνολογία έναντι των LIB.
Κατά τη διάρκεια της ιστορίας των μπαταριών τα τελευταία 200 χρόνια, η έρευνα για τα SIB πραγματοποιήθηκε με θέρμη δίπλα-δίπλα με την ανάπτυξη LIB. Η ηλεκτροχημική δραστηριότητα του TiS2 για το λίθιο και η σκοπιμότητά του για αποθήκευση ενέργειας παρουσιάστηκε για πρώτη φορά τη δεκαετία του 1970. Μετά από αυτή την ανακάλυψη, η ικανότητα των ιόντων Na να εισαχθούν στο TiS+2 έγινε αντιληπτή στις αρχές της δεκαετίας του 1980. Με την ανακάλυψη του γραφίτη ως υλικού ανόδου χαμηλού κόστους και μέτριας χωρητικότητας για τα LIB και την αποτυχία παρεμβολής ιόντων νατρίου, η ταχεία ανάπτυξη του LIB εμφανίστηκε τη δεκαετία του 1990, αντικαθιστώντας την ανάπτυξη στη χημεία νατρίου. Στη συνέχεια, το 2000, η διαθεσιμότητα για αποθήκευση νατρίου σε σκληρό άνθρακα (HC), η οποία θα παρείχε ενεργειακή ικανότητα παρόμοια με αυτή του Li σε γραφίτη, αναζωογόνησε το ερευνητικό ενδιαφέρον για τα SIB.
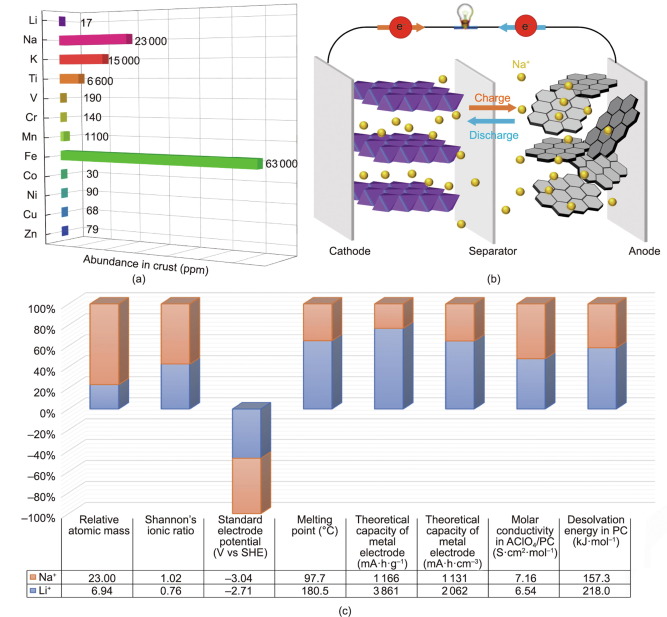
Σύγκριση μπαταρίας ιόντων νατρίου και μπαταρίας ιόντων λιθίου
Η αναβίωση των SIB -σε συνδυασμό με την ολοένα αυξανόμενη πίεση από την έλλειψη διαθεσιμότητας αποθεμάτων λιθίου και την αντίστοιχη κλιμάκωση του κόστους- παρέχει μια συμπληρωματική στρατηγική στα LIB. Οι SIB έχουν κερδίσει αυξανόμενη ερευνητική προσοχή, σε συνδυασμό με θεμελιώδη επιτεύγματα στην επιστήμη των υλικών, στην προσπάθεια να ικανοποιήσουν την αυξανόμενη διείσδυση των τεχνολογιών ανανεώσιμων πηγών ενέργειας. Τα στοιχεία του στοιχείου και οι μηχανισμοί ηλεκτροχημικής αντίδρασης των SIB είναι βασικά πανομοιότυπα με αυτά των LIB, εκτός από τον φορέα φορτίου, ο οποίος είναι Na στο ένα και Li στο άλλο. Ο κύριος λόγος για την ταχεία επέκταση της χημείας των υλικών SIB αποδίδεται στους παραλληλισμούς στις φυσικοχημικές ιδιότητες μεταξύ των δύο αλκαλικών μετάλλων.
Πρώτον, οι αρχές λειτουργίας και η κατασκευή κυψελών των SIB είναι παρόμοιες με εκείνες των εμπορικών LIB, αν και το Na χρησιμεύει ως φορέας φορτίου. Τέσσερα κύρια συστατικά υπάρχουν σε ένα τυπικό SIB: ένα υλικό καθόδου (συνήθως μια ένωση που περιέχει Na). ένα υλικό ανόδου (δεν περιέχει απαραίτητα Na). έναν ηλεκτρολύτη (σε υγρή ή στερεή κατάσταση). και ένα διαχωριστικό. Κατά τη διάρκεια της διαδικασίας φόρτισης, τα ιόντα νατρίου εξάγονται από τις καθόδους, οι οποίες είναι συνήθως στρωματοποιημένα οξείδια μετάλλων και πολυανιονικές ενώσεις, και στη συνέχεια εισάγονται στις άνοδοι, ενώ το ρεύμα ταξιδεύει μέσω ενός εξωτερικού κυκλώματος προς την αντίθετη κατεύθυνση. Κατά την εκφόρτωση, το Na αφήνει τις ανόδους και επιστρέφει στις καθόδους με μια διαδικασία που αναφέρεται ως «αρχή της κουνιστή καρέκλας». Αυτές οι ομοιότητες επέτρεψαν την προκαταρκτική κατανόηση και την ταχεία ανάπτυξη της τεχνολογίας SIB.
Επιπλέον, η μεγαλύτερη ιοντική ακτίνα Na φέρνει τα δικά της πλεονεκτήματα: αυξημένη ευελιξία ηλεκτροχημικής θετικότητας και μειωμένη ενέργεια αποδιαλυτοποίησης σε πολικούς διαλύτες. Το μεγαλύτερο κενό στην ιοντική ακτίνα μεταξύ του Li και των ιόντων μετάλλου μετάπτωσης συνήθως οδηγεί σε αστοχία της ευελιξίας του σχεδιασμού του υλικού. Αντίθετα, ένα σύστημα με βάση το νάτριο επιτρέπει πιο εύκαμπτες στερεές δομές από ένα σύστημα με βάση το λίθιο και διαθέτει τεράστια ιοντική αγωγιμότητα. Χαρακτηριστικό παράδειγμα είναι το β-Al2O3, για το οποίο η παρεμβολή Na έχει το τέλειο μέγεθος και υψηλή αγωγιμότητα. Οξείδια μετάλλων μεταπτώσεως με περισσότερα στρώματα με διαφορετικούς τρόπους στοίβαξης M+x+ μπορούν εύκολα να πραγματοποιηθούν σε ένα σύστημα με βάση το νάτριο. Ομοίως, η μεγάλη ποικιλία κρυσταλλικών δομών που είναι γνωστές για την οικογένεια ιοντικών αγωγών νατρίου (NaSICON) είναι πολύ πιο περίπλοκη από αυτή των αναλόγων λιθίου. Το πιο σημαντικό, μπορεί να επιτραπεί πολύ υψηλότερη ιοντική αγωγιμότητα στις ενώσεις NaSICON, η οποία υπερβαίνει κατά πολύ την ιοντική αγωγιμότητα σε ενώσεις ιοντικών αγωγών λιθίου (LiSICON).
Τελευταίο αλλά εξίσου σημαντικό, συστηματικές έρευνες με διαφορετικούς απρωτικούς πολικούς διαλύτες έχουν δείξει ότι η μεγαλύτερη ιοντική ακτίνα Na προκαλεί ασθενέστερη ενέργεια αποδιάλυσης. Το μικρότερο Li έχει υψηλότερη επιφανειακή πυκνότητα φορτίου γύρω από τον πυρήνα από το Na όταν και τα δύο έχουν το ίδιο σθένος. Επομένως, το Li σταθεροποιείται θερμοδυναμικά μοιράζοντας περισσότερα ηλεκτρόνια με τα μόρια του πολικού διαλύτη. Δηλαδή, το Li μπορεί να ταξινομηθεί ως ένας τύπος οξέος Lewis. Ως αποτέλεσμα, απαιτείται σχετικά υψηλή ενέργεια αποδιάλυσης για το εξαιρετικά πολωμένο Li, που οδηγεί σε σχετικά μεγάλη αντίσταση μεταφοράς που προκαλείται από τη μεταφορά του Li από την υγρή κατάσταση (ηλεκτρολύτη) στη στερεή κατάσταση (ηλεκτρόδιο). Δεδομένου ότι η ενέργεια αποδιάλυσης σχετίζεται στενά με την κινητική μεταφοράς που συμβαίνει στη διεπιφάνεια υγρού/στερεού, η σχετικά χαμηλή ενέργεια αποδιάλυσης είναι ένα σημαντικό πλεονέκτημα για το σχεδιασμό SIB υψηλής ισχύος.